مطالب مشابه
- برنامه و جدول واکسیناسیون کودکان
- روش های رایج برای سنجش آزمایشگاهی سطح ویتامین D
- اصول تغذیه دوران بارداری و شیردهی چگونه است؟
- برای غربالگری نوزادان چه آزمایش هایی پیشنهاد می شود؟
- مصرف مولتی ویتامین ها برای چه کسانی ضروری است؟
- برای تصفیه خون چه بخوریم؟
- مواد غذایی و تیروئید
- آزمایش DNA Fitچیست؟
- یک آزمایش خون جدید برای غربالگری 8 نوع سرطان
- تست قند خون ناشتا (FBG)
دسته بندی مطالب
همه چیز درباره ی کنترل متابولیسم و تعادل انرژی بدن
از نقطه نظر علم بیوشیمی، سلامتی انسان در گرو کیفیت عملکرد سلولهای بدن و طبیعی بودن واکنش ها و فرآیندهای شیمیایی مربوط به آنها است. از طرفی فعالیت مطلوب سلول ها و ایجاد تعادل و هماهنگی بین واکنش های مختلف بیوشیمیایی، وابسته به وجود ترکیبات آلی مانند کربوهیدرات ها، چربی ها، پروتئین ها، اسیدهای نوکلئیک و ریزمغذی هایی مانند ویتامین ها و مواد معدنی است که در کنار هورمونها و آنزیم های مختلف، هر یک دارای نقشی کلیدی و منحصر به فرد در کنترل متابولیسم و تعادل انرژی در بدن هستند.
رعایت اصل تعادل و تنوع در رژیم غذایی روزانه برای داشتن یک بدن طبیعی و سالم، امری ضروری و غیر قابل انکار است. در این مطلب سعی بر این است تا با مروری بر مفاهیم متابولیکی و نحوه کنترل آن، اهمیت تعادل انرژی و تنوع غذایی را با رویکردهای بیوشیمیایی بررسی نماییم.
بدن انسان و نیاز به تعادل انرژی، مسئله این است!
بدن انسان برای انجام کارهای مختلف از نشستن روی یک صندلی و انجام فعالیت های فکری تا پرداختن به فعالیت های سنگین ورزشی، واکنش های روحی و هیجانی، مقابله با انواع بیماری ها و حتی به هنگام استراحت و خوابیدن نیاز به کسب انرژی دارد. این انرژی از مصرف مواد غذایی مختلف به عنوان منابع سوختی تأمین می شود. به طور کلی، بیشتر مواد غذایی شامل سه دسته اصلی کربوهیدرات ها، چربی ها و پروتئین ها هستند که طی مراحل گوناگون به اجزای کوچک تری تجزیه شده و در نهایت سلول های بدن از آنها به عنوان سوخت برای تأمین انرژی مورد نیاز خود بهره مند می شوند.
از طرفی نیاز به انرژی برای هر یک از اندام ها و بافت های بدن انسان مانند مغز، ماهیچه ها، بافت چربی، کلیه ها، کبد، قلب، گلبول های قرمز و سیستم گوارشی بر اساس الگوی متابولیسمی متفاوتی که دارا هستند، متفاوت است، همچنین نیازهای غذایی بسته به شرایط مختلف مانند سیری و گرسنگی، چاقی و لاغری، مواجهه با انواع آسیب های فیزیکی مانند سوختگی، شکستگی و جراحی، انجام فعالیت های مختلف ورزشی اعم از قدرتی یا استقامتی و حتی در هنگام استراحت یا خواب عمیق بر اساس تغییرات و سازش های متابولیسمی متفاوت است؛ بنابراین شناخت مکانیسم های مختلف متابولیکی در بدن انسان می تواند در انتخاب یک رژیم غذایی متنوع، متعادل و متناسب راهگشا باشد.
متابولیسم یا سوخت و ساز سلولی
فرآیندی را که طی آن بدن انسان و سلول های شکل دهنده آن، مواد غذایی مصرفی را به انرژی موردنیاز خود تبدیل می نمایند، متابولیسم یا سوخت و ساز سلولی می نامیم که شامل واکنش های بسیار پیچیده بیوشیمیایی است. فرآیند متابولیسم و تغییر و تبدیل انرژی از تعداد زیادی مسیرهای متوالی و متعامل تشکیل شده است که واجد الگوهای مشترکی هستند و از راههای مختلف و متنوعی کنترل می شوند. استخراج انرژی از مواد غذایی شامل سه مرحله است؛ ابتدا مولکولهای بزرگ مواد غذایی مانند کربوهیدراتها، چربی ها و پروتئین ها به واحدهای کوچکتر سازنده خود یعنی گلوکز، اسیدهای چرب و آمینواسیدها شکسته می شوند. در مرحله دوم مولکولهای کوچک طی واکنش هایی به مولکول استیل کوآنزیم A تبدیل می شوند. مرحله سوم تحت عنوان چرخه کربس یا اسید سیتریک شناخته می شود که طی آن انرژ ATP تولید می گردد.
شکل 1. خلاصه ای از مسیرهای متابولیکی در بدن انسان
انواع واکنشهای متابولیکی
واکنش های متابولیکی را می توانیم به دو گروه عمده تقسیم نماییم؛ واکنش های آنابولیکی که با مصرف انرژی بر ساخت و ساز مولکول ها متمرکزند و واکنش های کاتابولیکی که با فرآیند هضم مواد غذایی و تجزیه مولکول ها جهت دریافت انرژی موردنیاز بدن مرتبط هستند. همچنین برخی از مسیرهای متابولیکی بسته به شرایط انرژی سلول می توانند آنابولیک یا کاتابولیک باشند که به عنوان مسیرهای آمفیبولیک نام برده می شوند. نکته قابل توجه از نقطه نظر بیوشیمیایی، مجزا بودن مسیرهای تجزیه ای و بیوسنتزی به دلایل انرژتیک سلولی است که در تسهیل فرآیند کنترل متابولیسم بدن مؤثر است. جهت برآورده سازی انرژی موردنیاز سلول ها، وجود هماهنگی و یکپارچگی بین مسیرهای متعدد متابولیکی لازم و ضروری است که این ویژگی به شکل کاملاً هوشمندانه در بدن انسان و سایر سیستم های زنده وجود دارد.
شکل 2. انواع واکنش های متابولیکی
ATP انرژی آزاد رایج عمومی در بدن انسان
انرژی حاصل از مصرف مواد غذایی به مولکولی به نام آدنوزین تری فسفات (ATP) که شکل رایج و عمومی انرژی آزاد در سیستم های زیستی است، منتقل می گردد. ATP به عنوان واحد انرژی اصلی درسلول بوده و مولکولی غنی از انرژی است و انرژی حاصل از هیدرولیز آن برای انجام فرآیندهای مختلف سلولی مورد استفاده قرار می گیرد. هنگامی که آدنوزین تری فسفات (ATP) به آدنوزین دی فسفات (ADP) یا آدنوزین مونو فسفات (AMP) هیدورلیز می شود، مقدار زیادی انرژی آزاد می گردد. این مولکول نوکلئوتیدی است که شامل یک آدنین، یک ریبوز و یک واحد تری فسفات است.
شکل 3. نمایی شماتیک از مولکول آدنوزین تری فسفات (ATP)
سایر ترکیبات فسفات دار پر انرژی
مولکول آدنوزین تری فسفات تنها ترکیب فسفات دار پر انرژی نیست. در واقع انرژی آزاد استاندارد هیدرولیز برخی از ترکیبات فسفریله در سیستم های زیستی مانند فسفوانول پیروات، 1 و 3- بیس فسفو گلیسرات و کراتین فسفات نسبت به ATP بیشتر است. توان حد واسط مولکول ATP در بین سایر مولکول های فسفریله باعث شده که ATP ، شکل انرژی آزاد رایج در بدن انسان و سایرسیستم های زیستی باشد و انرژی حاصل از کاتابولیسم به این مولکول منتقل گردد. ویژگی های ساختاری مولکول ATP و محصولات ناشی از هیدرولیز آن باعث شده است که این مولکول به عنوان دهنده مؤثر گروه فسفریل و دهنده سریع انرژی آزاد عمل نماید.
سوخت های اصلی متابولیک در بدن انسان
بعد از اکسیژن و آب به عنوان مهم ترین عوامل حیات، بدن انسان باید به سایر ترکیبات مانند کربوهیدرا تها (قندها)، لیپیدها (چربی ها) ، اسیدهای چرب، پروتئین ها، ویتامین ها، مواد معدنی و فیبرها دسترسی داشته باشد. در این بین، کربوهیدرات ها، چربی ها و پروتئینها که همگی از مواد آلی هستند به عنوانسه گروه اصلی از مواد غذایی به شمار می آیند (شکل 4). با مصرف کافی و متعادل این منابع سوختی مهم، انرژی موردنیاز اندا مها و سلولهای بدن تأمین می گردد. این سه گروه اصلی که بیشترین حجم مواد غذایی را تشکیل می دهند باید قبل از جذب و استفاده شدن، به واحدهای تشکیل دهنده خود یعنی مونوساکاریدها، اسیدهای چرب و اسیدهای آمینه هیدرولیز شوند.
شکل 4. به طور کلی، بیشتر مواد غذایی در سه دسته اصلی کربوهیدراتها، پروتئین ها و انواع روغن های طبقه بندی می شوند.
.
ماده سوختی مهم به نام گلوکز یا قند خون
اکثر انسان ها در رژیم غذایی خود از مقادیر قابل توجهی کربوهیدارت های پیچیده یا نشاسته ای استفاده می کنند. این ترکیبات برای اینکه به وسیله روده قابلیت جذب داشته باشند، باید به قندهای ساده تر یا مونوساکاریدها تبدیل شوند. آنزیم آمیلاز بزاق و پانکراس هیدورلیز ترکیبات نشاسته ای را کاتالیز می کنند. مونوساکاریدها مانند گلوکز یا فروکتوز به درون سلول های روده منتقل شده و سپس وارد جریان خون می شوند. گلوکز به دلایل بیوشیمیایی و ساختاری در بین سایر مونوساکاریدها، یک ماده سوختی مهم به شمار می آید و اکثر بافت های بدن به آن نیازمندند. از نظر اهمیت بالینی، گلوکز مهم ترین مونوساکارید بوده و قسمت اصلی کربوهیدرات های مواد غذایی به صورت گلوکز وارد جریان خون می شوند. این مونوساکارید سوخت اصلی بافت های بدن انسان و سایر پستانداران است. در مغز، این نیاز اساسی بوده و تنها ماده سوختی است که این اندام تحت شرایط غیر گرسنگی از آن استفاده می کند. در سلول های قرمز خون نیز گلوکز تنها ماده سوختی است که در همه شرایط مورد استفاده قرار می گیرد. همچنین گلوکز به عنوان سوخت عمومی جنین شناخته می شود.
سایر مونوساکاریدهای سوختی
در کنار گلوکز به عنوان مهم ترین و پرمصرف ترین منبع سوختی، سایر مونوساکاریدها مانند گالاکتوز و فروکتوز (قند میوه) نیز منابع سوختی مهمی هستند. نکته قابل توجه در این مورد این است که مسیرهای کاتابولیکی برای متابولیزه شدن گالاکتوز و فروکتوز وجود نداشته و لذا این دو قند باید به متابولیت های گلوکز تبدیل شوند. به عبارت کلی، طی فرآیندهای متابولیکی، تمامی کربوهیدرا تها در نهایت به گلوکز یا قند خون تبدیل شده که سوخت و ساز یا متابولیسم آن به دو طریق هوازی و بی هوازی در بدن انجام می شود. هر سه مونوساکارید گلوکز، فروکتوز و گالاکتوز در گروه مونوساکاریدهای 6 کربنی (هگزوزها) قرار می گیرند.
شکل 5. مونوساکاریدها
مسیر اصلی متابولیسم گلوکز موجود در رژیم غذایی
گلیکولیز، مسیر اصلی متابولیسم گلوکز و سایر مونوساکاریدها مانند فروکتوز و گالاکتوز را در رژیم غذایی فراهم می آورد. این فرآیند در انسان و بسیاری از موجودات به عنوانیک مسیر مهم و اساسی تبدیل انرژی به حساب می آید. در این مسیر متابولیکی که کنترل آن را در سطح بافت های ماهیچه اسکلتی و کبد می توان در نظر گرفت، گلوکز تجزیه می شود تا ATP موردنیاز ساخته شود. این مسیر در ماهیچه ها انرژی لازم جهت انقباض عضلانی را فراهم می کند و بر اساس نیاز به ATP ، تنظیم می گردد. تنظیم مسیر گلیکولیز در بافت کبد نیز بسیار پیچیده است.
بافت کبد در کنار بسیاری از اعمال بیوشیمیایی متنوع خود، سطح قند خون را ثابت نگاه می دارد؛ به این شکل که در هنگام افزایش قند خون آن را به شکل گلیکوژن ذخیره می کندو زمانی که سطح قند خون پایین باشد، گلوکز را از محل ذخایر خود به جریان خون رها می سازد تا انرژی موردنیاز بافت های بدن تأمین گردد. گلیکولیز توالی از 10 واکنش است که در سیتوزول سلول روی می دهد و در نهایت گلوکز به پیرووات تبدیل شده و طی آن مولکول های ATP تولید می شوند. پیروواتی که در سیتوزول تشکیل می شود به داخل میتوکندری منتقل شده و به طریقه اکسیداتیو به استیل کوآنزیم A دکربوکسیله شده و وارد چرخه اسید سیتریک (چرخه کربس یا چرخه اسید تری کربوکسیلیک) می شود که مسیر نهایی اکسیداسیون کربوهیدرات ها، چربی هاو پروتئین هاو در نهایت تولید ATP است. تحت شرایط بی هوازی مثلاً در هنگام انجام فعالیت های ورزشی قدرتی، پیرووات به لاکتات تبدیل می گردد (شکل 6).
شکل 6. خلاصه ای از فرآیندهای گلیکولیز و چرخه کربس
نقش ویتامین ها و مواد معدنی در کنترل متابولیسم
ویتامین ها و مواد معدنی، ترکیباتی هستند که وجود آنها جهت انجام فعالیت های متابولیکی و بیوشیمیایی بدن ضروری بوده و می بایست از طریق رژیم غذایی فراهم شوند. دریافت ناکافی این ترکیبات زمینه ساز بیماری های مختلف شده و زیاده روی در مصرف آنها نیز ممکن است باعث مسمومیت شود. این گروه از ترکیبات دارای نقش های متفاوت و مهمی از جمله به عنوان کوآنزیم ها و کوفاکتورهای آنزیمی، تنظیم بروز ژن، تمایز سلولی، هوموستاز سلولی، آنتی اکسیدانی، تأمین انرژی، متابولیسم مواد سه گانه (کربوهیدرات ها، چربی ها، پروتئین ها)، تنظیم چرخه سلولی، فعالیت شبه هورمونی و غیره هستند که خود دلیلی بر اهمیت نقش متابولیکی این ترکیبات در تأمین و تعادل انرژی است.
از نقطه نظر متابولیسم تأمین انرژی، ویتامین های گروه B مانند B1 (تیامین)، B2(ریبوفلاوین)، B3 ( نیاسین) B5 (اسید پانتوتنیک) در چرخه کربس یا اسید سیتریک دارای نقش های کلیدی هستند. اشاره شد که ATP به عنوان واحد انرژی اصلی در سلول بوده و مولکولی غنی از انرژی است؛ به عبارت دیگر ATP یک حامل فعال شده گرو ههای فسفریل محسوب می شود، زیرا انتقال گروه فسفریل از این مولکول یک فرآیند انرژی زا است. نکته قابل توجه این است که بسیاری از حاملین فعال شده ای که به عنوان کوآنزیم عمل می کنند از ویتامین های محلول در آب بخصوص ویتامین های گروه B مشتق می شوند (شکل 7). انواع دیگری از ویتامین ها مانند ویتامین های E،D،C،A و K نقش کوآنزیمی نداشته و دارای اعمال متفاوت دیگری هستند.
شکل 7. بسیاری از حاملین فعال شده در متابولیسم نقش کوآنزیمی دارند. کوآنزیم ها که از ویتامین های محلول در آب مشتق می شوند.
منابع سوختی تأمین کننده انرژی در اندام های مختلف بدن انسان
از نقطه نظر بیوشیمیایی، هر یک از اندام های بدن انسان جهت تأمین انرژی موردنیاز خود از منابع سوختی، به شکل متفاوتی عمل می نمایند؛ به عنوانمثال در حالت سیری و عدم نیاز به مصرف مواد غذایی، مولکول گلوکز تنها منبع سوختی برای بافت مغز است. در گرسنگی های طولانی مدت مثل حالت روزه داری، اجسام کتونی که در بافت کبد تولید می شوند تا حدودی جایگزین گلوکز شده و به عنوان سوخت غالب مغز به کار گرفته می شوند (شکل 8). نکته قابل توجه اینکه مغز از چربی ها و اسیدهای چرب به عنوان منبع سوختی استفاده نمی کند. بههنگام گرسنگی های طولانی مدت یا برخی از اختلالات متابولیکی مانند دیابت نوع دو کنترل نشده که غلظت اجسام کتونی تولیدشده در بافت کبد در جریان خون افزایش می یابد، بافت مغز از اجسام کتونی به عنوان سوخت جایگزین گلوکز استفاده می نماید.
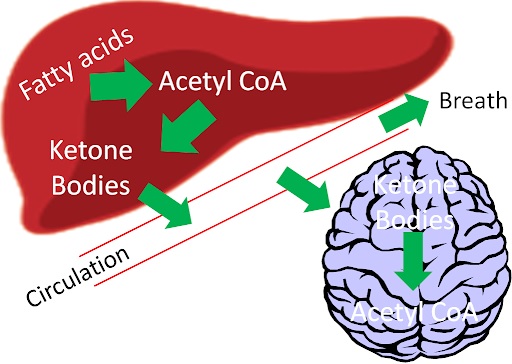
شکل 8. در برخ مواقع بافت مغز از اجسام کتونی به عنوان سوخت جایگزین گلوکز استفاده می نماید.
گلوکز، اسیدهای چرب و اجسام کتونی، سوخت های عمده ماهیچه های اسکلتی هستند. ماهیچه های اسکلتی بدن از گلوکز در فعالیتهای ناگهانی و از اسیدهای چرب در حالت استراحت به عنوان سوخت های ترجیحی استفاده می نمایند. در بافت قلب برخلاف ماهیچه های اسکلتی، ذخیره گلیکوژنی وجود ندارد و اسیدهای چرب منبع اصلی سوخت قلب هستند. البته بافت قلب از اجسام کتونی و همچنین از لاکتات نیز به عنوان منابع سوختی استفاده می نماید. در بافت چربی، تری آسیل گلیسرول های ذخیره شده، به عنوان منبع مهم سوختی به شمار می آیند.
در کلیه ها، ریه ها، گلبولهای قرمز و دستگاه گوارش نیز گلوکز به عنوانمنبع سوختی اصلی به شمار می آید. بافت کبد که نقشی استراتژیک و اساسی در کنترل و یکپارچگی متابولیسم بدن ایفا می نماید، برای تأمین انرژی مورد نیاز خود تا حد امکان در مصرف مواد سوختی مانند گلوکز صرفه جویی کرده و فعالیت های متابولیکی متنوع آن بیشتر در جهت حمایت، پشتیبانی و تأمین انرژی سایر اندامها مثل مغز و ماهیچه ها است.
به منظور برآورده کردن نیازهای گلوکز سایر اندام ها، بافت کبد به سرعت می تواند ذخایر گلیکوژن خود را طی فرآیند گلیکوژنولیز تجزیه نموده و گلوکونئوژنز که فرآیند ساخت گلوکز از پیشسازهای غیر کربوهیدراتی است را انجام دهد، همچنین کبد نقشی مهم در تنظیم متابولیسم چربی ها ایفا می نماید. در حالت سیری و عدم نیاز غذایی، اسیدهای چرب سنتزشده در بافت کبد به بافت چربی فرستاده می شوند. در حالت گرسنگی طولانی مدت، اسیدهای چرب توسط کبد به اجسام کتونی تبدیل می شوند.
عدم استفاده بافت های بدن از آمینواسیدها به عنوان منابع سوختی
اگرچه پروتئین ها بخصوص در بافت ماهیچه از ذخایر سوختی محسوب می شوند، ولی استفاده از این ماکرومولکول ها جهت تأمین انرژی موردنیاز بافت های بدن، تهدیدی جدی برای حیات انسان است، بنابراین مکانیسم هایی هوشمندانه ای برای جلوگیری از مصرف آمینواسیدها به عنوان منابع سوختی در بدن انسان طرح ریزی شده است، به عنوان مثال در طی گرسنگی های طولانی مدت، مکانیسم های کنترل متابولیسم، مصرف سوخت را به سمت استفاده بیشتر از چربی ها سوق می دهد و با راهکارهایی مانند اکسیداسیون اجسام کتونی در بافت مغز در مجموع به حفظ و نگهداری پروتئین ها کمک می نمایند. وجود آمینواسیدها برای سنتز پروتئین ها و همچنین به عنوان پیش ساز ترکیبات مهمی دیگر چون پورین ها، پیریمیدیدن ها و هورمون هایی مانند اپی نفرین، تیروکسین و نوروترانسمیترها و غیره ضروری است. برخی از این آمینواسیدها که بافت های بدن قادر به سنتز آنها نیستند و به عنوان اسیدهای آمینه ضروری شناخته می شوند، لازم است تا از طریق مصرف مواد غذایی تأمین شوند.
بیشتر آمینواسیدهای دریافتی از رژیم غذایی و یا حاصل از تجزیه پروتئین های بافتی به همراه گلیسرول حاصل از تجزیه تری آسیل گلیسرول ها می توانند در فرآیند گلوکونئوژنز مورد استفاده قرار گیرند. آمینواسیدهایی که تولید استیل کوآنزیم A می کنند، تحت عنوان اسیدهای آمینه کتوژنیک خوانده می شوند. در شرایط روزه داری و گرسنگی طولانی مدت، از استیل کوآنزیم A برای سنتز اجسام کتونی در کبد استفاده می شود. بافت کبد در متابولیسم آمینواسیدهای مواد غذایی یک نقش اساسی ایفا می کند. اولویت استفاده از آمینواسیدها به جای کاتابولیسم، به کارگیری آنها در سنتز پروتئین ها است؛ بنابراین آمینواسیدها به جای استفاده به عنوان یک ماده سوختی به سمت سنتز پروتئین های موردنیاز بدن هدایت می شوند. نکته قابل توجه اینکه آلفا کتواسیدهای ناشی از تجزیه آمینواسیدها خود از مواد سوختی کبد به شمار می آیند.
کنترل متابولیسم در حالت های سیری و گرسنگی
هورمون های انسولین و گلوکاگون دو تنظی مکننده مهم متابولیسم بدن انسان در شرایط سیری یا حالتی که پس از مصرف مواد غذایی وجود دارد، هستند. در واقع ترشح هورمون انسولین که به روش های گوناگونی ذخیره سازی مواد سوختی و سنتز پروتئین ها را تحریک می کند پیام آور حالت سیری است. هنگامی که پس از صرف غذا، سطح گلوکز خون افزایش می یابد، ترشح انسولین و افزایش غلظت آن ورود گلوکز به بافت ماهیچه را افزایش داده و باعث تحریک سنتز گلیکوژن در ماهیچه ها می شود، همچنین سطح بالای انسولین باعث ورود گلوکز به بافت چربی شده و گلیسرول -3 فسفات موردنیاز در سنتز تری آسیل گلیسرولها را فراهم می آورد. فعالیت انسولین در متابولیسم آمینواسیدها و پروتئین ها نیز مؤثر است.
این هورمون برداشت آمینواسیدهای شاخه دار مانند والین، لوسین و ایزولوسین را توسط ماهیچه ها افزایش داده و ساخته شدن پروتئین در ماهیچه ها را تسهیل می نماید. در حالت گرسنگی اولیه و کاهش سطح گلوکز خون، ترشح هورمون گلوکاگون باعث تجزیه ذخایر گلیکوژن شده و به دنبال آن مقادیر زیادی گلوکز از کبد به خون آزاد می شود. ورود گلوکز به ماهیچه ها و بافت چربی در پاسخ به سطح پایین انسولین کاهش می یابد. در شرایط سیری و پس از صرف یک وعده غذایی، ذخایر کافی کربوهیدرات وجود دارد و سوخت متابولیکی برای بیشتر بافت های بدن، گلوکز است. در حالت گرسنگی شدید و روزه داری، گلوکز باید برای استفاده مغز و گلبول های قرمز که هر دو به مقادیر زیادی وابسته به گلوکز هستند، تقسیم شود؛ بنابراین بافت هایی مانند ماهیچه ها و کبد که می توانند از سوخت های متابولیکی دیگر به جز گلوکز بهره مند شوند، از اسیدهای چرب به عنوانسوخت استفاده می کنند، همچنین، کبد اجسام کتونی را از اسیدهای چرب ساخته و به عضله و سایر بافت ها می فرستد.
اهمیت وعده صبحانه در تنظیم متابولیسم بدن
اگرچه اندام های مختلف بدن به هنگام استراحت و خواب شبانه به مانند روز و بیداری فعال نیستند، ولی کماکان برای ادامه حیات، وظایف خود را به آرامی انجام م یدهند؛ بنابراین هر یک از اندام های بدن مانند مغز، قلب، ریه ها، دستگاه گوارش، کبد، کلیه ها و حتی ماهیچه های بدن در طول شب و حین خواب جهت انجام اعمال خود به انرژی نیاز دارند. اشاره شد که گلوکز یا قند خون به عنوان مهم ترین منبع سوختی برای سلول های بدن است و مصرف مقدار کافی و متعادل آن برای تأمین انرژی ضروری است. مولکول های گلوکز در بافت کبد طی فرایند گلیکوژنز به شکل گلیگوژن ذخیره شده و در زمان نیاز به انرژی، مثلاً بین وعده های غذایی، هنگامی گرسنگی یا روزه داری و خواب شبانه، زنجیره های گلیکوژن طی فرآیند گلیکوژنولیز شکسته شده و جهت تأمین انرژی به واحدهای منفرد گلوکز تبدیل می شوند (شکل 9).
شکل 9. خلاصه ای از دو فرآیند گلیکوژنز و گلیکوژنولیز
همانطوری که قبلاً نیز اشاره شد، به جز حالت گرسنگی های طولانی مدت، تنها ماده سوختی مغز انسان گلوکز است. از طرفی مغز فاقد هرگونه ذخیره سوختی بوده و بدین ترتیب به ذخیره ای همیشگی از گلوکز نیازمند است. در گرسنگی های طولانی مدت و یا به هنگام خواب شبانه به دلیل عدم مصرف مواد غذایی و کاهش میزان قند خون و متعاقب آن کاهش ذخایرِ گلیکوژن در بافت کبد، سیستم ایمنی بدن انسان به طور هوشمندانه ای احساس خطر کرده و در مصرف سوخت گلوکز و ذخایر آن صرف هجویی می نماید. به همین دلیل گنجاندن مواد غذایی شیرین مانند عسل و خرما در وعده صبحانه توجیه مناسبی برای افزایش میزان قند خون و تأمین انرژی موردنیاز بدن برای ادامه فعالیت های روزانه است. بر همین اساس، با حذف اشتباه وعده صبحانه یا مصرف اندک آن که متأسفانه در برخی از رژیم های غذایی دیده می شود، علاوه بر اینکه انرژی موردنیاز برای سلول های بدن در طول روز تأمین نمی گردد و باعث خستگی و افت کیفیت کار و فعالیت روزانه افراد می شود، با کاهش یافتن متابولیسم و سوخت و ساز بدن که به دلایل سیستم ایمنی ذکر شد، زمینه برای مصرف بیشتر مواد قندی و شیرینی ها در طول روز فراهم شده و در نهایت ریسک ابتلا به چاقی را افزایش می بخشد.
علاوه بر این، عدم تأمین سطوح کافی و متعادل از گلوکز در رژیم غذایی روزانه بر کیفیت خواب شب نیز اثر گذاشته و اثرات منفی آن بر فعالیت های انسان در ساعات بیداری و روز مشاهده خواهد شد. توجه به ساعت بیولوژیک یا ساعت زیستی بدن نیز که کنتر لکننده چرخه ای از فرآیندهای متابولیکی و بیوشیمیایی مانند ترشح هورمو نها، سیری، گرسنگی، خواب و غیره است و تحت عنوان چرخه روزانه یا سیرکادین ( Circadian rhythm ) نامیده می شود، نیز در روند کنترل متابولیسم و تعادل انرژی حائز اهمیت است. عادت به تغذیه ب یبرنامه و صرف وعده های غذایی بدون توجه به ساعت زیستی بدن، علاوه بر به هم خوردن تعادل هورمون ها و اختلال در روند فرآیندهای متابولیکی زمان بندی شده مانند چرخه خواب، زمینه ساز چاقی و سایر اختلالات متابولیک است. بدیهی است زمانی که از مصرف مواد غذایی از جمله ترکیبات قندی صحبت م یکنیم، اصل بر وجود یک بدن سالم و طبیعی است، چرا که در افرادی که دارای بیماری های زمینه ای مانند دیابت، قلبی و عروقی و غیره هستند، الگوی مصرف مواد غذایی متفاوت و با نظر پزشک معالج تعیین می شود؛ بنابراین مطابق با اصل تنوع و تعادل در رژیم غذایی، همانطوریکه مصرف بیش از حد مواد غذایی برای سلامتی انسان خطرآفرین است، مصرف ناکافی نیز می تواند باعث بروز مشکلات جدی در بدن انسان شود.
کنترل متابولیسم به هنگام کاهش ذخایر گلیکوژن کبدی
اشاره شد که فرآیند گلیکولیز در بسیاری از موجودات از جمله انسان یک مسیر تبدیل انرژی بوده و طی واکنش های متوالی جهت تولید ATP ، مولکول گلوکز تجزیه و به پیرووات تبدیل می شود، همچنین در شرایط بی هوازی و در برخی میکروارگانیسم ها، محصول نهایی لاکتات است که یک نقطه پایانی در متابولیسم بوده و به عنوان یک منبع انرژی برای برخی اندام ها به شمار می آید. طی فرآیندی به نام گلوکونئوژنز، سنتز گلوکز از منابع غیر کربوهیدراتی مانند لاکتات، آمینواسیدها و گلیسرول میسر می گردد. فرآیند گلوکونئوژنز بخصوص در طی گرسنگی های طولانی مدت و روز هداری و با توجه به اینکه گلوکز به عنوانسوخت اصلی مغز است و همچنین سلول های قرمز خون تنها گلوکز را به عنوانسوخت مورد استفاده قرار می دهند بسیار حائز اهمیت است. تعدادی از واکنش هایی که پیرووات را به گلوکز تبدیل می کنند با مسیر گلیکولیز مشترک هستند. جایگاه اصلی گلوکونئوژنز، کبد بوده و وجود آن به حفظ سطح قند خون و تأمین منابع انرژی برای فعالیت اندام هایی چون مغز و عضلات کمک می نماید. ترکیبات اصلی برای فرآیند گلوکونئوژنز در بافت کبد عبارتند از لاکتات و آلانین که در عضلات اسکلتی از پیرووات تولید می شوند. طی فرآیندی تحت عنوان چرخه کوری، لاکتات تشکیل شده در عضلات فعال، توسط کبد به گلوکز تبدیل می شود (شکل 10 ).
شکل 10 . چرخه کوری عضله اسکلتی در حال انقباض، لاکتات را در اختیار کبد قرار می دهد و این اندام از آن برای سنتز گلوکز استفاده می نماید.
تعادل انرژی و تنظیم وزن بدن
یکی از مهم ترین عوامل تهدیدکننده سلامت بشر چاقی و اضافه وزن است که بخصوص در جوامع پیشرفته به یک اپیدمی تبدیل شده است. افزایش مصرف مواد غذایی پرکالری و عدم فعالیت فیزیکی که منجر به عدم تعادل بین کالری دریافتی و کالری مصرفی می شود، از دلایل اصلی بروز چاقی و اضافه وزن است. این کالری اضافی که به صورت چربی در بدن انسان ذخیره می شود، به عنوانیک عامل خطر در بروز بیماری هایی مانند دیابت، فشارخون، قلبی و عروقی، انواع سرطان و اختلالات عضلانی و اسکلتی شناخته می شود. تغییر در سبک زندگی و رعایت یک رژیم غذایی متنوع و متعادل در کنار انجام فعالیت های ورزشی متناسب و مداوم و کنترل هوشمندانه استرس، ابزار مناسبی جهت کنترل سوخت و ساز و ثابت نگهداشتن سطح انرژی و کنترل اشتها در بدن انسان است.
بافت چربی که حین چاقی و اضافه وزن افزایش می یابد، از سلول هایی به نام آدیپوسیتها تشکیل یافته که جهت ذخیره سازی انرژی به بهترین شکل ممکن تخصص یافته اند. اهمیت وجود این سلول ها در این است که با ذخیره کردن انرژی به صورت مولکول های چربی باعث می شوند که انسان و سایر جانداران برای کسب انرژی موردنیاز خود، دائماً در حال مصرف مواد غذایی نباشند و این کار در وعده های زمانی مشخصی در طول شبانه روز انجام شود. نکته مهم و حیاتی در قابلیت ذخیره سازی انرژی اضافی در بافت چربی این است که در صورت اختلال در این فرآیند، تجمع چربی در سایر بافت های بدن اتفاق افتاده و منجر به بروز انواع بیماری ها مانند کبد چرب می شود که تهدیدکننده جدی برای سلامتی انسان است.
بر اساس این رویکرد، به نظر می رسد که وجود بافت چربی در حالت فیزیولوژیک می تواند از تجمع چربی اضافی در سایر سلول ها ممانعت کرده و به حفظ تعادل انرژی و عملکرد مطلوب سایر بافت ها کمک نماید. در این بین مدیریت سیستم عصبی، سیستم غدد درو نریز و سیستم ایمنی به عنوانسه ضلع یک مثلث و ارتباط و هماهنگی آنها نقش مهمی را در کنترل اشتها، تنظیم تعادل انرژی و وزن بدن انسان ایفا می نمایند. بر همین اساس هنگامی که بدن انسان در حالت گرسنگی قرار دارد و یا زمانی که میزان کالری مصرف شده از کالری دریافتی بیشتر باشد، ترشح هورمونی به نام لپتین که گاهی هورمون سیری نیز نامیده می شود از سلول های بافت چربی کاهش می یابد. سطوح کاهش یافته هورمون لپتین که میزان ترشح آن توسط بافت چربی، نسبت مستقیم با توده چربی بدن دارد، می تواند باعث افزایش اشتها و میل به مصرف مواد غذایی گردد. این هورمون با ارسال پیام به هیپوتالاموس در مغز اشتها را کنترل نموده و جهت تنظیم میزان انرژی مصرفی در روز، به مغز کمک می کند.
از نکات قابل توجه در افرادی که دچار عارضه چاقی هستند، کاهش حساسیت به لپتین و افزایش مقاومت به این هورمون است که باعث ایجاد اختلال در فرآیند انتقال سیگنال شده و به عبارتی، پیام توقفِ خوردن به مغز نمی رسد. این موضوع می تواند زمینه ساز بروز سایر بیماری های متابولیک مانند مقاومت به انسولین یا سندرم متابولیک شود که در آن غلظت قند خون و انسولین به میزان قابل توجهی افزایش می یابد. مصرف متعادل کربوهیدرات ها از جمله فروکتوز و ساکارز و کاهش مصرف نوشیدنی های قندی و چربی های با ترانس بالا می تواند به تعدیل میزان انسولین و بهبود وضعیت هورمون لپتین کمک نماید.
لازم به ذکر است که دو هورمون انسولین و لپتین در تنظیم هموستازی انرژی و کنترل اشتها نقش مهمی بر عهده دارند. انسولین هورمونی است که توسط سلول های بتا در لوزالمعده تولید می شود و اصلی ترین هورمون جهت ذخیره شدن چربی در بدن است. از طرفی، هورمونی به نام گرلین یا هورمون گرسنگی، هنگامی که معده خالی است، ترشح می شود که عملکرد آن رساندن پیام گرسنگی به هیپوتالاموس مغز است. پایین بودن این هورمون در افراد چاق چه در حالت گرسنگی و چه بعد از صرف غذا، باعث اختلال در ارسال پیام سیری و توقف خوردن به هیپوتالاموس می شود.
شکل 11 . نقش هورمون های لپتین، انسولین و گرلین در تعادل انرژی
کنترل متابولیسم در حین فعالیت های ورزشی
ورزشکاران جهت عملکرد مطلوب و استفاده بهینه از حداکثر توان بدنی خود نیازمند به انتخاب مواد سوختی مناسب جهت تأمین انرژی موردنیاز ماهیچه های اسکلتی در حین فعالیت های بدنی اعم از هوازی یا بی هوازی هستند. هوازی یا بی هوازی بودن فعالیت های ورزشی به نوع واکنش های متابولیکی که انرژی موردنیاز ماهیچهها را تولید می کنند، مرتبط است. نوع مواد سوختی جهت تأمین انرژی مورد نیاز ورزشکار بر اساس شدت و مدت زمان فعالیت ورزشی متفاوت است. از نقطه نظر بیوشیمیایی، فعالیت انقباضی و تأمین انرژی حرکتی ماهیچه ها مستلزم اتصال پروتئین های حرکتی از جمله میوزین به مولکول های ATP و هیدرولیز آن است. نکته قابل توجه در حین انجام ورزش های هوازی و استقامتی مانند دوی ماراتن یا ورزش های بیهوازی و قدرتی مانند دوی 100متر، نحوه تولید مقادیر لازم از مولکو لهای ATP جهت تأمین نیروی کافی برای فعالیت انقباضی ماهیچه ها در بازه زمانی مناسب است.
همانطوری که قبلاً نیز اشاره شد، توان حد واسط مولکولهای ATP در بین سایر مولکول های فسفریله باعث شده که ATP شکل انرژی آزاد رایج در سیستم های زیستی باشد، ولی این مولکول تنها ترکیب فسفاتدار پر انرژی نیست و ترکیبات دیگری مانند کراتین فسفات (فسفوکراتین) نیز وجود دارند که قادر به انتقال سریع گروه فسفریل به مولکول ADP و تولید ATP هستند. از طرفی ذخایر ATP و کراتین فسفات در ماهیچه ها محدود بوده و تنها ظرف چند ثانیه مصرف می شوند، از این رو جهت حفظ سرعت و قدرت عضلانی در طول یک فعالیت ورزشی قدرتی مثل دوی سرعت 100 متر که تنها چند ثانیه زمان لازم دارد، لازم است تا منابع سوختی دیگری به جز ATP ذخیره شده و کراتین فسفات مورد استفاده قرار گیرند، بر همین اساس، گلیکولیز بی هوازی ذخایر گلیکوژن ماهیچه ها و تولید لاکتات می تواند به تولید مقادیر بیشتری از ATP کمک نماید؛ بنابراین، ماده سوختی اصلی در شروع یک فعالیت ورزشی یا در طی ورزش های بی هوازی، قدرتی و سنگین از گلیکوژن ماهیچه ها تأمین می شود.
در طی ورزش بیهوازی، ذخایر گلیکوژن کبد و ماهیچه به علت آزادسازی کاتکول آمینها کاهش می یابد. میزان ذخایر گلیکوژن بافت ماهیچه تا حد زیادی به رژیم غذایی وابسته است. انتخاب یک رژیم غذایی با مقادیر کافی از کربوهیدراتها در حفظ مقادیر گلیکوژن ماهیچه ها در طول ورزش های بیهوازی و سنگین مؤثر است؛ در مقابل به جهت مصرف سریع ذخایر ATP و کراتین فسفات و همچنین ایجاد اسیدوز لاکتیک که یک عامل محدودکننده برای پیشرفت گلیکولیز در ورزش های بی هوازی محسوب می شود، در ورز شهای هوازی و طولانی مدت نیازی به تولید مولکول های ATP از طریق انجام واکنش های بی هوازی نیست؛ به عنوان مثال، یک دونده ماراتن که باید مسافتی حدود 42 کیلومتر را ظرف مدت زمان 2 ساعت طی نماید، به مواد سوختی دیگری نیاز دارد. در فعالیت های هوازی، بخشی از ATP موردنیاز می بایست اکسیداسیون کامل گلیکوژن ماهیچه و کبد تأمین شود که باز هم جوابگوی ATP موردنیاز برای یک فعالیت مستمر 2 ساعته نبوده و در اینجا اهمیت بافت چربی و هماهنگی آن با بافت های ماهیچه وکبد مشخص می شود. تولید ATP موردنیاز برای فعالیت های ورزشی طولانی مدت مانند دوی ماراتن از اکسیداسیون اسیدهای چرب حاصل از تجزیه چربی ها در بافت چربی حاصل می شود.
نکته بسیار مهم و حیاتی در حین فعالیت های طولانی مدت ورزشی، نحوه استفاده ترکیبی بهینه از مواد سوختی است تا علاوه بر برقراری تعادل انرژی و عملکرد مطلوب در طول فعالیت ورزشی، در انتها مقادیر کافی از قند خون در اختیار ورزشکار وجود داشته باشد؛ به عبارت دیگر در حین انجام فعالیت های ورزشی طولانی مدت و هوازی هیچ سوختی به طور انحصاری مصرف نشده و بافت ماهیچه از همه منابع سوختی در زمان های مناسب به شکل بهینه استفاده می کند. سطح پایین قند خون و افزایش ترشح هورمون گلوکاگون نسبت به هورمون انسولین باعث آزاد شدن اسیدهای چرب از بافت چربی و ورود آنها به ماهیچه ها می شود. با اکسیداسیون اسیدهای چرب، ورود گلوکز به چرخه کربس کاهش یافته و تعادل غلظت قند خون در پایان فعالیت طولانی مدت ورزشی حفظ می شود.
شکل 12 . در ورزشهای قدرتی مانند دوی 100 متر انرژی مورد نیاز ورزشکار از ATP، کراتین فسفات و گلیکولیز و ذخایر گلیکوژن ماهیچه ها تأمین می شود.
کنترل متابولیسم در حالت تروما
در علم پزشکی هر نوع ضربه، شوک و آسیب که از خارج به بدن وارد شود مانند سوختگی، شکستگی یا جراحت، تروما (Trauma) نامیده می شود. آگاهی از تغییرات متابولیکی و نوع نیازهای تغذیه ای در شرایط تروما، در تسریع روند بهبود بیماران از اهمیت بسزایی برخوردار است؛ به عنوان مثال یکی از تغییرات مهم و حیاتی در حین یک ترومای شدید، کاهش وزن به علت افزایش کاتابولیسم پروتئین های بافتی است که معمولاً به دنبال استراحت های طولانی مدت در بستر و به دلیل آتروفی عضلات پدید می آید. این روند باعث ایجاد موازنه منفی نیتروژن در بیماران شده که می بایست در طول دوره نقاهت با انتخاب یک رژیم غذایی مناسب برطرف گردد.
نکته قابل توجه این است که علی رغم افزایش تجزیه پروتئین ها در طول تروما که خود به دلیل افزایش روند گلوکونئوژنز است، لیکن پروتئین هابه عنوانمنبع اصلی تأمین انرژی محسوب نمی شوند. تحت این شرایط نیز به مانند وضعیت گرسنگی شدید، چربی های موجود در بافت چربی به عنوان منبع عمده انرژی عمل می نمایند. دانستن این تغییرات متابولیکی به انتخاب یک رژیم غذایی مناسب جهت تسریع روند بهبود بیماران کمک می نماید. انتخاب یک رژیم غذایی مناسب که بتواند پروتئین های کافی را به بدن بیمار برساند، در بازگرداندن وزن از دست رفته بیمار و ایجاد موازنه مثبت نیتروژن راهگشا خواهد بود. لازم به ذکر است که کمبود آمینواسیدها می تواند منجر به توازن منفی نیتروژن در بدن انسان شود. در این حالت پروتئین های بیشتری تجزیه می گردد و در نتیجه دفع نیتروژن از جذب آن بیشتر می شود. در بدن انسان برخی از آمینواسیدها که به نام آمینواسیدهای ضروری شناخته می شوند، می بایست از طریق رژیم غذایی دریافت گردند. مابقی آمینواسیدها که غیرضروری هستند در بدن انسان و از حدواسط های چرخه کربس و سایر مسیرها ساخته می شوند.
نیتروژن یک جزء اصلی از آمینواسیدها است و منبع آن برای تمام آمینواسیدها به شکل آمونیاک است. آمینواسیدها که اجزای ساختمانی پروتئین ها هستند برای بسیاری از مولکول های مهم دیگر نیز مانند نوکلئوتیدها و نوروترانسمیترها به عنوان منبع نیتروژن هستند. اسکلت کربنی آمینواسیدها نیز از مسیر گلیکولیزی، مسیر پنتوز فسفات یا چرخه کربس حاصل می شود. بیوسنتز آمینواسیدها ارتباط تنگاتنگی با تغذیه دارد، زیرا بدن انسان توانایی تولید برخی از آمینواسیدها را ندارد و بنابراین باید مقادیر کافی را از طریق رژیم غذایی مناسب دریافت نماید.
بدن انسان برای رشد و عملکرد مناسب نیاز به ۲۰ اسیدآمینه متفاوت دارد. ۹ اسید آمینه شامل هیستیدین، ایزولوسین، لوسین، لیزین، متیونین، فنیل آلانین، ترئونین، تریپتوفان و والین به عنوان اسیدهای آمینه ضروری طبقه بندی می شوند که برخلاف اسیدهای آمینه غیرضروری، بدن قادر به سنتز آنها نبوده و باید از طریق رژیم غذایی و یا مکم لهای غذایی دریافت شوند. آرژنین، آمینواسیدی است که در یک فرد بالغ مقادیر کافی آن از طریق چرخه اوره تأمین می گردد ولی این مقدار برای یک کودک در حال رشد کافی نیست و باید از طریق خوراکی تأمین گردد.
شکل 13 . اسیدهای آمینه ترکیباتی هستند که از اتم های نیتروژن، کربن، هیدروژن واکسیژن تشکیل می شوند.
بحث و نتیجه گیری
حیات انسان بعد از نیاز به آب و اکسیژن، به مصرف ترکیباتی مانند کربوهیدرات ها، چرب یها، پروتئین ها، فیبرها، ویتامین ها و مواد معدنی وابسته است که می بایست از طریق مصرف مواد غذایی مختلف تأمین شوند. فعالیت های مختلف روزانه اعم از جسمی و فکری و همچنین فعالیت ارگان های داخلی بدنمانند مغز، قلب، ریه ها، کلیه ها، کبد، ماهیچه ها و غیره نیاز به انرژی دارد. دریافت انرژی مورد نیاز فرآیندهای حیاتی با تغذیه متناسب و کافی مبتنی بر اصل تنوع و تعادل مواد غذایی تأمین خواهد شد. عملکرد مطلوب فرآیندهای متابولیکی و سوخت و ساز سلولی که به استفاده از منابع غذایی به عنوان مواد سوختی و دریافت انرژی موردنیاز از آنها وابسته است، تضمینی بر تندرستی و سلامت جسم و روح در دوران های مختلف زندگی انسان است. سلول های بدن انسان جهت انجام فعالیت های خود و حفظ فرآیندهای حیاتی، از مولکول های ATP به عنوان انرژی رایج و عمومی استفاده می کنند.
از نقطه نظر ترمودینامیکی، استفاده بهینه از منابع سوختی، جهت تأمین انرژی و حفظ تعادل آن موضوعی مهم و حیاتی است که میتواند به کاهش بی نظمی یا آنتروپی در بدن انسان کمک نماید. موضوع عدم تعادل انرژی و زیاده روی در مصرف مواد غذایی و تولید رادیکال های آزاد و ذخیره شدن بیش از حد انرژی در سلول های بدن که منجر به چاقی، دیابت، بیماریهای قلبی و عروقی، برخی از انواع سرطانها و غیره می شود تا فقر غذایی به علت تخلیه منابع انرژی بدن که می تواند به اختلالات رشد و نقص سیستم ایمنی منجر شود، امروزه به یک چالش اساسی و تهدید کننده سلامتی انسان در سطح جهان تبدیل شده است.
بر اساس ترکیبات موجود در مواد غذایی، مسیرهای متابولیکی شامل مسیرهای آنابولیکی، کاتابولیکی و آمف یبولیکی در بافت های بدن تعیین می شوند. افزایش آگاهی ما از نقش مواد سوختی مختلف و تغییرات متابولیسمی طبیعی بدن مانند آنچه در شرایط سیری و گرسنگی و فعالیت های ورزشی هوازی و بی هوازی اتفاق می افتد، زمینه مناسبی را برای درک بهتر شرایط متابولیسمی بدن در حالت های غیرطبیعی و بیماری فراهم می آورد. بافت های کبد و ماهیچه های اسکلتی، انرژی را به صورت مولکول های قند و بافت چربی انرژی را به صورت مولکول های چربی در خود ذخیره می کنند.
قندها و چربی ها مهم ترین مولکول های انرژی زا محسوب شده و در کنترل متابولیسم، تعادل انرژی و عملکرد سلول های بدن دارای نقش کلیدی هستند، لیکن تداوم ذخیره سازی و بیش و کم هر یک منجر به بر هم ریختن هموستازی کالریک و ایجاد اختلالات متابولیکی خواهد شد، به عنوان مثال افزایش گلوکز بیش از نیاز سلولها، منجر به بیماری دیابت و افزایش بیش از حد چربی منجر به چاقی و زمینه ساز بیماری های قلبی و عروقی و غیره است، لذا کافی بودن مقدار انرژی دریافتی موجود در رژیم غذایی جهت عملکرد مطلوب اندام های مختلف بدن و توجه به رعایت اصل تنوع و تعادل غذایی و همچنین تناسب غذایی بر حسب سن، جنس، میزان فعالیت بدنی و سایر شرایط فیزیولوژیکی در کنار سایر پارامترهای سبک زندگی متعادل، ابزاری مهم در کنترل متابولیسم و حفظ تعادل انرژی و در نهایت رفاه جسم و روح انسان است.
References:
Biochemistry, 6TH Edition, 2007, by Jeremy M. Berg, John L.Tymoczko & Lubert Stryer
Harper’s Illustrated Biochemistry, 28TH Edition, 2009 by Robert K. Murray, David A. Bender, Kathleen M. Botham, Peter J.Kennelly, Victor W.Rodwell, P. Anthony Weil
Henry’s Clinical Diagnosis and Management by Laboratory Methods,21TH, 2007 by Matthew R. Pincus Richard A. McPherson
Tietz Textbook of Clinical Chemistry and Molecular Diagnostics, 4TH Edition, 2006 by Carl A. Burtis, David E Bruns & Edward R Ashwood__
نویسنده